Skandium, met elementsimbool Sc en atoomgetal 21, is maklik oplosbaar in water, kan met warm water in wisselwerking tree en verdonker maklik in die lug. Die hoofvalensie daarvan is +3. Dit word dikwels gemeng met gadolinium, erbium en ander elemente, met 'n lae opbrengs en 'n inhoud van ongeveer 0.0005% in die kors. Skandium word dikwels gebruik om spesiale glas en liggewig hoëtemperatuurlegerings te maak.
Tans is die bewese skandiumreserwes in die wêreld slegs 2 miljoen ton, waarvan 90~95% in Bauxiet-, fosforiet- en yster-titaanerts voorkom, en 'n klein deel in uraan-, torium-, wolfram- en seldsame aarderts, hoofsaaklik versprei in Rusland, China, Tadjikistan, Madagaskar, Noorweë en ander lande. China is baie ryk aan skandiumbronne, met enorme mineraalreserwes wat verband hou met skandium. Volgens onvolledige statistieke is die skandiumreserwes in China ongeveer 600 000 ton, wat voorkom in Bauxiet- en fosforietafsettings, porfier- en kwartsaar-wolframafsettings in Suid-China, seldsame aardertafsettings in Suid-China, Bayan Obo-seldsame aard-ysterertsafsetting in Binne-Mongolië, en Panzhihua vanadium-titaanmagnetietafsetting in Sichuan.
As gevolg van die skaarste van skandium, is die prys van skandium ook baie hoog, en op sy hoogtepunt was die prys van skandium tot 10 keer die prys van goud opgeblaas. Alhoewel die prys van skandium gedaal het, is dit steeds vier keer die prys van goud!
Ontdek Geskiedenis
In 1869 het Mendeleev 'n gaping in atoommassa tussen kalsium (40) en titaan (48) opgemerk, en voorspel dat daar ook 'n onontdekte intermediêre atoommassa-element hier was. Hy het voorspel dat die oksied daarvan X₂OÅ is. Skandium is in 1879 deur Lars Frederik Nilson van die Universiteit van Uppsala in Swede ontdek. Hy het dit uit die swart seldsame goudmyn onttrek, 'n komplekse erts wat 8 tipes metaaloksiede bevat. Hy het dit onttrekErbium(III)oksiedvan swart seldsame gouderts, en verkryYtterbium(III)oksiedvan hierdie oksied, en daar is nog 'n oksied van 'n ligter element, waarvan die spektrum toon dat dit 'n onbekende metaal is. Dit is die metaal wat deur Mendeleev voorspel is, waarvan die oksied isSc₂O₃Die skandiummetaal self is vervaardig uitSkandiumchlorieddeur elektrolitiese smelting in 1937.
Mendeleev
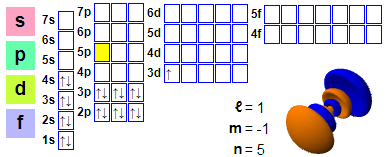
Elektronkonfigurasie
Elektronkonfigurasie: 1s² 2s² 2p6 3s² 3p6 4s² 3d1
Skandium is 'n sagte, silwerwit oorgangsmetaal met 'n smeltpunt van 1541 ℃ en 'n kookpunt van 2831 ℃.
Vir 'n aansienlike tydperk na die ontdekking daarvan, is die gebruik van skandium nie gedemonstreer nie as gevolg van die moeilikheid in produksie. Met die toenemende verbetering van seldsame aardelement-skeidingsmetodes, is daar nou 'n volwasse prosesvloei vir die suiwering van skandiumverbindings. Omdat skandium minder alkalies is as yttrium en lantaanied, is die hidroksied die swakste, dus sal die gemengde mineraal wat seldsame aardelemente bevat, van die seldsame aardelement geskei word deur die "stap-presipitasie"-metode wanneer skandium(III)hidroksied met ammoniak behandel word nadat dit in oplossing oorgedra is. Die ander metode is om skandiumnitraat te skei deur polêre ontbinding van nitraat. Omdat skandiumnitraat die maklikste is om te ontbind, kan skandium geskei word. Daarbenewens is die omvattende herwinning van gepaardgaande skandium uit uraan, torium, wolfram, tin en ander mineraalafsettings ook 'n belangrike bron van skandium.
Nadat 'n suiwer skandiumverbinding verkry is, word dit omgeskakel in ScCl₃Å en saam met KCl en LiCl gesmelt. Die gesmelte sink word as die katode vir elektrolise gebruik, wat veroorsaak dat skandium op die sinkelektrode neerslaan. Dan word die sink verdamp om metaalagtige skandium te verkry. Dit is 'n liggewig silwerwit metaal met baie aktiewe chemiese eienskappe, wat met warm water kan reageer om waterstofgas te genereer. Dus word die metaalskandium wat jy in die prentjie sien, in 'n bottel verseël en met argongas beskerm, anders sal skandium vinnig 'n donkergeel of grys oksiedlaag vorm en sy blink metaalglans verloor.
Toepassings
Beligtingsbedryf
Die gebruike van skandium is gekonsentreer in baie helder rigtings, en dit is nie 'n oordrywing om dit die Seun van die Lig te noem nie. Die eerste magiese wapen van skandium word 'n skandiumnatriumlamp genoem, wat gebruik kan word om lig aan duisende huishoudings te bring. Dit is 'n metaalhalied-elektriese lig: die gloeilamp word gevul met natriumjodied en skandiumtrijodied, en skandium- en natriumfoelie word gelyktydig bygevoeg. Tydens hoëspanningsontlading straal skandiumione en natriumione onderskeidelik lig van hul kenmerkende emissiegolflengtes uit. Die spektrale lyne van natrium is 589.0 en 589.6 nm, twee bekende geel ligte, terwyl die spektrale lyne van skandium 361.3~424.7 nm is, 'n reeks van naby ultraviolet- en blou liguitstraling. Omdat hulle mekaar aanvul, is die algehele ligkleur wat geproduseer word wit lig. Dit is juis omdat skandiumnatriumlampe die eienskappe van hoë ligdoeltreffendheid, goeie ligkleur, kragbesparing, lang lewensduur en sterk misbrekende vermoë het, dat hulle wyd gebruik kan word vir televisiekameras, pleine, sportlokale en padbeligting, en staan bekend as die derde generasie ligbronne. In China word hierdie tipe lamp geleidelik as 'n nuwe tegnologie bevorder, terwyl hierdie tipe lamp in sommige ontwikkelde lande reeds in die vroeë 1980's wyd gebruik is.
Die tweede magiese wapen van skandium is sonfotovoltaïese selle, wat die lig wat op die grond versprei word, kan versamel en dit in elektrisiteit kan omskep om die menslike samelewing aan te dryf. Skandium is die beste versperringsmetaal in metaalisolator-halfgeleier-silikon-sonselle en sonselle.
Die derde magiese wapen word 'n γA-straalbron genoem. Hierdie magiese wapen kan op sy eie helder skyn, maar hierdie soort lig kan nie met die blote oog ontvang word nie; dit is 'n hoë-energie fotonvloei. Ons onttrek gewoonlik 45Sc uit minerale, wat die enigste natuurlike isotope van skandium is. Elke 45Sc-kern bevat 21 protone en 24 neutrone. 46Sc, 'n kunsmatige radioaktiewe isotoop, kan as γ-stralingsbronne gebruik word, of spooratome kan ook gebruik word vir radioterapie van kwaadaardige gewasse. Daar is ook toepassings soos yttrium, gallium, skandium en granaatlaser.Skandiumfluoriedglas infrarooi optiese vesel, en skandiumbedekte katodestraalbuis op televisie. Dit lyk asof skandium met helderheid gebore word.
Legeringsbedryf
Skandium in sy elementêre vorm word wyd gebruik vir die dotering van aluminiumlegerings. Solank 'n paar duisendstes skandium by aluminium gevoeg word, sal 'n nuwe Al3Sc-fase gevorm word, wat 'n metamorfose-rol in aluminiumlegering sal speel en die struktuur en eienskappe van die legering aansienlik sal verander. Deur 0.2%~0.4% Sc by te voeg (wat baie soortgelyk is aan die verhouding van sout by gebraaide groente tuis, slegs 'n bietjie is nodig) kan die herkristallisasietemperatuur van die legering met 150-200 ℃ verhoog word, en hoëtemperatuursterkte, strukturele stabiliteit, sweisprestasie en korrosieweerstand aansienlik verbeter. Dit kan ook die brosheidsverskynsel vermy wat maklik voorkom tydens langtermynwerk by hoë temperature. Hoësterkte en hoë taaiheid aluminiumlegering, nuwe hoësterkte korrosiebestande sweisbare aluminiumlegering, nuwe hoëtemperatuur aluminiumlegering, hoësterkte neutronbestralingsbestande aluminiumlegering, ens., het baie aantreklike ontwikkelingsvooruitsigte in lugvaart, lugvaart, skepe, kernreaktore, ligte voertuie en hoëspoedtreine.
Skandium is ook 'n uitstekende modifiseerder vir yster, en 'n klein hoeveelheid skandium kan die sterkte en hardheid van gietyster aansienlik verbeter. Boonop kan skandium ook as 'n toevoeging vir hoëtemperatuur-wolfram- en chroomlegerings gebruik word. Natuurlik, benewens die maak van trouklere vir ander, het skandium 'n hoë smeltpunt en is die digtheid daarvan soortgelyk aan aluminium, en word dit ook gebruik in liggewiglegerings met 'n hoë smeltpunt soos skandium-titaniumlegering en skandium-magnesiumlegering. As gevolg van die hoë prys word dit egter oor die algemeen slegs in hoë-end vervaardigingsnywerhede soos ruimtependeltuie en vuurpyle gebruik.
Keramiekmateriaal
Skandium, 'n enkele stof, word oor die algemeen in legerings gebruik, en die oksiede daarvan speel op 'n soortgelyke wyse 'n belangrike rol in keramiekmateriale. Die tetragonale sirkonium-keramiekmateriaal, wat as 'n elektrodemateriaal vir vasteoksiedbrandstofselle gebruik kan word, het 'n unieke eienskap waar die geleidingsvermoë van hierdie elektroliet toeneem met toenemende temperatuur en suurstofkonsentrasie in die omgewing. Die kristalstruktuur van hierdie keramiekmateriaal self kan egter nie stabiel bestaan nie en het geen industriële waarde nie; dit is nodig om sekere stowwe te doteer wat hierdie struktuur kan vasstel om sy oorspronklike eienskappe te behou. Die byvoeging van 6~10% skandiumoksied is soos 'n betonstruktuur, sodat sirkonium op 'n vierkantige rooster gestabiliseer kan word.
Daar is ook ingenieurskeramiekmateriale soos hoësterkte- en hoëtemperatuurbestande silikonnitried as verdigters en stabiliseerders.
As 'n verdichter,Skandiumoksiedkan 'n vuurvaste fase Sc2Si2O7 aan die rand van fyn deeltjies vorm, wat die hoëtemperatuurvervorming van ingenieurskeramiek verminder. In vergelyking met ander oksiede kan dit die hoëtemperatuurmeganiese eienskappe van silikonnitried beter verbeter.
Katalitiese chemie
In chemiese ingenieurswese word skandium dikwels as 'n katalisator gebruik, terwyl Sc2O3 gebruik kan word vir dehidrasie en deoksidasie van etanol of isopropanol, ontbinding van asynsuur, en die produksie van etileen uit CO en H2. Die PtAl-katalisator wat Sc2O3 bevat, is ook 'n belangrike katalisator vir swaar olie-hidrogeneringssuiwering en raffineringsprosesse in die petrochemiese industrie. In katalitiese krakreaksies soos Cumeen, is die aktiwiteit van die Sc-Y-zeolietkatalisator 1000 keer hoër as dié van die aluminiumsilikaatkatalisator; In vergelyking met sommige tradisionele katalisators, sal die ontwikkelingsvooruitsigte van skandiumkatalisators baie helder wees.
Kernenergiebedryf
Deur 'n klein hoeveelheid Sc2O3 by UO2 in hoëtemperatuurreaktor-kernbrandstof te voeg, kan roostertransformasie, volumetoename en krake wat deur UO2 na U3O8-omskakeling veroorsaak word, vermy word.
Brandstofsel
Net so sal die byvoeging van 2,5% tot 25% skandium by nikkel-alkalibatterye hul lewensduur verhoog.
Landbouteling
In die landbou kan sade soos mielies, beet, ertjies, koring en sonneblom met Scandiumsulfaat behandel word (die konsentrasie is gewoonlik 10-3~10-8mol/L, verskillende plante sal verskil), en die werklike effek van die bevordering van ontkieming is bereik. Na 8 uur het die droë gewig van wortels en knoppe met onderskeidelik 37% en 78% toegeneem in vergelyking met saailinge, maar die meganisme word nog bestudeer.
Van Nielsen se aandag aan die skuld van atoommassa-data tot vandag, het skandium slegs vir 'n honderd of twintig jaar mense se visie betree, maar dit het amper vir 'n honderd jaar op die bank gesit. Dit was eers met die kragtige ontwikkeling van materiaalwetenskap in die laat vorige eeu dat dit hom vitaliteit gebring het. Vandag het seldsame aardelemente, insluitend skandium, warm sterre in materiaalwetenskap geword, wat steeds veranderende rolle in duisende stelsels speel, elke dag meer gerief in ons lewens bring en ekonomiese waarde skep wat selfs moeiliker is om te meet.
Plasingstyd: 29 Junie 2023